| 일 | 월 | 화 | 수 | 목 | 금 | 토 |
|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 8 | 9 | 10 | 11 | 12 | 13 | 14 |
| 15 | 16 | 17 | 18 | 19 | 20 | 21 |
| 22 | 23 | 24 | 25 | 26 | 27 | 28 |
- dispersion
- Zirconia
- X7T
- mlcc
- oxygen vacancy
- Sintering
- CERAMIC
- Barium titanate
- CSZT
- nano powder
- Powder
- microstructure
- bme
- paste
- ni-paste
- Automotive
- NI-MLCC
- hydrothermal
- halt
- C0G
- core-shell
- EV
- coating
- ZrO2
- X8R
- Murata
- reliability
- nickel
- ASSB
- BaTiO3
- Today
- Total
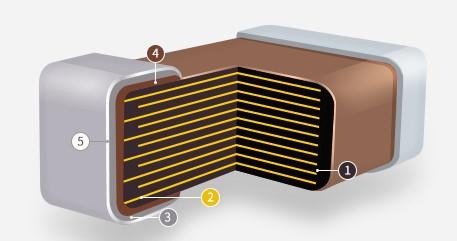
MLCC Material & Process
(Paste)용제계에서의 안료분산 본문
色材, 77〔8〕 (2004)
小林敏勝
1. 용제계에서의 안료분산의 특징
안료분산은 도료나 잉크, 그림물감 등의 제조에 있어서 중요한 공정이며, 그 좋고나쁨은 상품의 광택이나 착색력, 은폐력, 채도 등의 광학적 성질, 유동성과 레벨링성 등의 레올로지적 성질, 침강이나 부츠 발생, 광차, 증점 등의 상품안정성에 막대한 영향을 미친다.
통상, 안료 메이커로 제조된 안료는, 건조해, 1차 입자(주 1)가 다수 응집한 상태로 안료 분산 공정에 제공된다.이것을, 비히클 안에서 이상적으로는 1차 입자의 상태까지 해응집해 안정화시키는 공정이 안료 분산 공정이다(주 2).따라서 예를 들어 평균 입자경이 100nm의 안료분산계가 필요한 경우에는 1차 입자경이 100nm 이하인 안료분체를 입수해야 한다. 최근의 고성능 분산기로는 1차 입자도 파쇄 가능한 경우가 있는데, 1차 입자가 파쇄되었을 때에는 파쇄면에 활성 부위가 생겨 분산계의 이상점도 증가가 발생하거나 최종 피막의 내후성이나 내구성에 문제가 생길 가능성이 높다.
안료 분산 공정은 Wetting, 기계적 해쇄, 분산 안정화의 세 개의 단위 과정으로 분할해 생각하면 분산 설계나 트러블 슈팅 시에 편리하다. 즉, 안료 분산 공정에서는 제일 먼저 건조해 응집한 1차 입자응집체의 비히클에 대한 wetting이 생긴다. 특히 1차 입자응집체 안에 있는 미세한 틈으로 비히클을 모세관 침투하는 것이 중요하다. 응집 부분이 비히클에 젖어 1차 입자 간 부착력이 감소한 상태에서 분산기의 비틀림이나 충격력이 더하면 더 작은 응집체로 분할된다.이 과정은 기계적 해체 과정이다.
이 과정은 분산기의 성능, 밀베이스의 점도 등의 인자에 영향을 받아 화학공학적인 접근이 중요하다. 보다 작은 응집체로 분할되면 비히클/안료 입자 계면의 면적이 증가하므로, 이 계면이 불안정한 경우에는 모처럼 분할된 입자끼리의 재응집이 생겨 분산이 진행되지 않는다.분산을 진행시키기 위해서는 비히클/안료 계면을 안정화시킬 필요가 있으며, 고분자 흡착층이나 전기 이중층을 안료 입자 주위에 형성시킴으로써 안정화가 달성되고 있다.이 과정이 분산 안정화 과정이다. 젖은 기계적 해체, 분산 안정화의 모든 과정이 만족받으면 이상적으로는 일정한 1차 입자의 분산계를 얻을 수 있을 것이다.
기계적 해쇄 과정에서는 앞서 기술한 바와 같이 화학공학적 접근이 중요하며, 본 연재 강좌에서는 분산기에 관한 별도 강의가 준비되어 있다.이 때문에, 본강에서는 기계적 해쇄 과정에 관한 해설은 할애한다.
일반적인 용제계의 도료나 잉크에서는 유기용제의 표면장력이 낮기 때문에, wetting 과정의 진행이 저해되어 분산이 진행되지 않는다는 것은 거의 생각할 수 없으며, 대부분의 경우 분산안정화의 과정을 어떻게 만족시킬 것인가가 중요하다.이 때문에, 이하에서는 용제계에서의 분산 안정화의 생각이나 수단에 대해 소개하기로 한다.
2.안료·고분자·용제의 친화성의 기본적인 생각
용제계의 도료나 잉크 등 실용적인 계열에서의 안료의 분산안정화는 안료 입자 주위에 고분자 흡착층을 형성시킴으로써 달성된다. 따라서 안료표면과 고분자의 친화성을 확보하고, 고분자의 흡착이 진행되기 쉽게 설계하는 것이 중요한데, 용제와 고분자, 용제와 안료표면과의 친화성도 시야에 넣어 이것을 생각할 필요가 있다. 그림 1을 참조하기 바란다
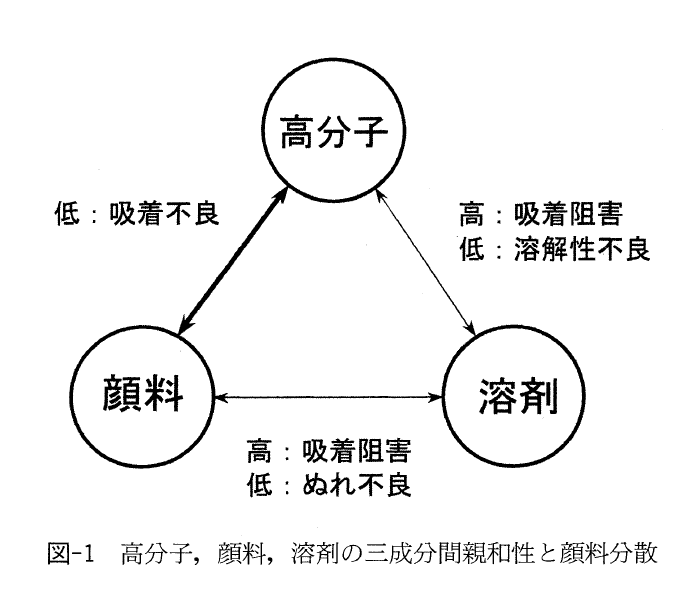
고분자가 안료에 흡착하기 위해서는, 안료와 고분자의 친화성은 용제와 고분자의 친화성보다 높을 필요가 있지만, 고분자 흡착을 우선하는 나머지, 안료에 대한 용제의 친화성이 너무 낮으면, 분산의 단위과정인 Wetting이 진행되지 않는다. 반면, 흡착한 고분자 사슬은 용매화되어, 용제중에 녹아 들어갈 필요가 있다.이를 위해서는 고분자와 용제의 사이에 친화성이 있어야 하지만 친화성이 너무 크면 고분자의 용제 안에 대한 분배계수가 커져 안료에 대한 흡착이 저해된다.
그럼, 구체적으로 어떻게 친화성을 생각하면 좋은가 라는 것이 되는데, 이 점에 관해서는 표1을 참조하기 바란다.열역학에 따르면 흡착이나 젖은 용해 등 어떤 현상을 생각하더라도 그 현상이 생기는 전후의 Gibb 자유에너지 변화(G)는 (-) 값을 받아야 한다. 엔탈피변화(△H)와 엔트로피변화(△S)를 이용해 T를 절대온도로 하면

성립하는 것이 현상 진행을 위한 필수 용건이다. 여기서, 흡착에서는 현상의 진행에 의해 계통의 난잡함이 감소한다. 즉 △S<0이기 때문에 △G<0을 위해서는 △H<0일 필요가 있다. 즉 친화성으로서는 발열적인 상호작용이 생기지 않으면 흡착이라는 현상은 진행되지 않게 된다. 반면 용해나 Wetting은 현상의 진행에 의해 계의 엔트로피가 증가하므로 1T S<0이며 G<0을 위해서는 T △S의 절대값을 넘지 않는 범위내에서 △H는 정값도 취하는 것이 허용된다. 즉 흡열적인 약한 상호작용에서도 현상이 진행되게 된다. 오히려 흡착을 저해하지 않도록 발열적인 상호작용을 피하고 0교비유적으로 말하면 흡착은 고분자와 안료 사이가 좋지 않으면 절대 진행되지 않지만 안료의 용제에 대한 목욕이나 고분자의 용해는 용제와의 사이가 그렇게 나쁠 수 없다는 얘기다.
19.2.2 번역중
'Material' 카테고리의 다른 글
| (C0G MLCC) 환원분위기에서 소성한 (CaSr)(TiZr)O3계 유전체의 저주파 유전 분산 (0) | 2021.05.01 |
|---|---|
| (Paste)잉크제조법과 생산기술 (0) | 2021.04.03 |
| (Material) 결합제 각론 (세라믹용 바인더) (0) | 2021.03.30 |
| (Material)Sekisui PVB Binder (0) | 2021.03.30 |
| (Powder Synthesis)박층 MLCC의 실현을 위한 티탄산바륨(BaTiO3)의 고도화 (0) | 2021.03.30 |